リチウム元素の性質と用途
元素リチウムを理解する
リチウムとは
原子番号3、記号Liのリチウムは、周期表で最も軽い金属であり、アルカリ金属である。リチウムは、実験室の珍品として存在していた2世紀の間に、世界的に取引される工業商品へと発展しました。今日、塩の電気分解やスポジュメンなどの鉱物の粉砕を通じたリチウムの精製と生産は、エネルギー貯蔵、宇宙開発、エレクトロニクスにおいて数十億ドル規模の産業の基礎となっている。

化学的性質
リチウムの化学的性質は、その物理的性質と同様に特徴的である:
-反応性:リチウムは水と激しく反応し、水酸化リチウム(LiOH)と水素ガスを生成する。例えば、小さなリチウムのかけらを水に沈めると、数秒以内に目に見える発泡が起こります。
-アルカリ性:アルカリ性:アルカリ金属であるリチウムは、外側の電子1個を容易に手放してLi⁺イオンを生成するため、リチウムイオン電池を含む電気化学反応において重要な役割を果たす。
- 引火性:リチウムは特徴的な赤い炎で発火するため、技術者はバルク・リチウムの取り扱いや保管の際に留意しなければならない。
物性データ表
|
物性値 |
値 |
|
原子番号 |
3 |
|
原子量 |
6.94 g/mol |
|
融点 |
180.54 °C |
|
沸点 |
1590 °C |
|
密度 |
0.534 g/cm³ |
|
外観 |
銀白色の金属 |
|
硬度 |
柔らかい |
|
電気伝導率 |
高い |
|
熱伝導率 |
高い |
リチウムの発見
リチウムは1817年、スウェーデンのウト島にあるペタライトから初めて発見された。Arfvedsonの分析により、ナトリウムやカリウムとは異なる性質を持つ未同定の新元素が発見されました。その後、リチウム塩の電気分解によって金属リチウムが分離され、科学者やエンジニアはその物理的・化学的特性をさらに分析できるようになった。やがて、リチウムの軽さ、高い反応性、電気化学的ポテンシャルという奇妙な組み合わせは、エネルギー貯蔵から工業用グリースや医薬品へとリチウムを軌道に乗せた。
合金とリチウム化合物
- リチウムアルミニウム合金:非常に軽量で硬く、航空機部品やスポーツカー部品に使用される。
- リチウム銅合金:電気伝導性が向上し、電子コネクターや回路によく使用される。
- リン酸鉄リチウム (LiFePO₄):安定性とサイクル寿命の長さから、電気自動車用バッテリーの正極によく使用される。
- 水酸化リチウム(LiOH)と炭酸リチウム(Li₂CO₃):充電池、潤滑油、工業化学プロセスにおいて重要。
- 塩化リチウム(LiCl):乾燥剤、エアコン、化学合成に使用。
例えば、テスラをはじめとする電気自動車メーカーは、安全性と機能性を保証するために熱安定性とエネルギー密度が最も重要なリン酸鉄リチウム(LFP)バッテリーを特定の自動車に採用している。
一般的な用途
リチウムにはさまざまな用途がある:
1.電池:リチウムイオン電池とリチウムポリマー電池は、その高いエネルギー密度により、携帯電子機器、電気自動車、再生可能エネルギー貯蔵システムにおいて市場を独占している。
2.合金:リチウムはアルミニウムや銅合金を軽くし、強度を失うことなく航空宇宙効率を向上させる。
3.医薬用途:炭酸リチウムは双極性障害の患者を安定させる。
4.耐熱ガラスとセラミックス:リチウムは耐熱衝撃性と強度を高める。
5.潤滑グリース:リチウムグリースは高温・高圧で優れた性能を発揮し、製造業や自動車産業で不可欠である。
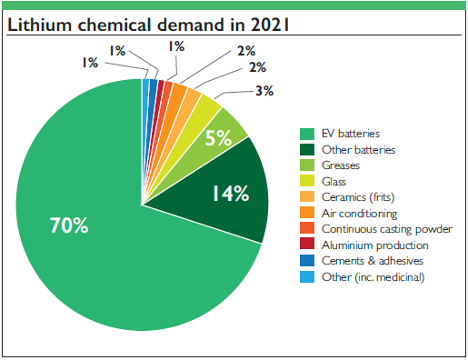 [1]
[1]
調製プロセス
リチウムは主に以下の方法で得られる:
1.リチウム金属は、電気分解によってLiClまたはLiFから回収され、市場用途の高純度が得られる。
2.鉱物の採掘:スポジュメンとペタライトは、炭酸リチウムまたは水酸化リチウムに加工され、電池や化学製品の製造に使用されます。
よくある質問
リチウムの最も頻繁な用途は何ですか?
主に充電式電池、軽合金、潤滑油、医薬品です。
リチウムはどのように採掘されますか?
リチウム塩の電気分解、またはスポジュメン鉱石から。
リチウムは反応性か?
はい、特に水と反応し、LiOHと水素ガスを形成します。
リチウムイオン電池とは何ですか?
高いエネルギー密度と長いサイクル寿命により、スマートフォン、ノートパソコン、電気自動車、再生可能エネルギー貯蔵システムに電力を供給しています。
参考文献
[1]国際リチウム協会(2023年10月13日).リチウム101.2025 年 7 月 17 日、https://lithium.org/lithium-101/から取得。

 バー
バー
 ビーズと球体
ビーズと球体
 ボルト&ナット
ボルト&ナット
 坩堝
坩堝
 ディスク
ディスク
 繊維
繊維
 映画
映画
 フレーク
フレーク
 フォーム
フォーム
 フォイル
フォイル
 顆粒
顆粒
 ハニカム
ハニカム
 インク
インク
 ラミネート
ラミネート
 しこり
しこり
 メッシュ
メッシュ
 メタライズド・フィルム
メタライズド・フィルム
 プレート
プレート
 粉類
粉類
 ロッド
ロッド
 シーツ
シーツ
 単結晶
単結晶
 スパッタリングターゲット
スパッタリングターゲット
 チューブ
チューブ
 洗濯機
洗濯機
 ワイヤー
ワイヤー
 コンバータと計算機
コンバータと計算機
 私たちのために書く
私たちのために書く




 Chin Trento
Chin Trento



